Ферментами в клетке могут быть белки липиды. Липиды. Состав и строение белков
Липиды представляют собой достаточно сложные по химической структуре вещества. В их состав также входят углерод, кислород, водород, но в отдельные группы липидов могут входить и фосфор, и сера, и азот (фосфатиды, пигменты). Все липиды гидрофобны, т.е. не растворяются в воде. Функции у липидов различны в зависимости от химического строения. Липиды не являются биополимерами.
Липиды классифицируются на 5 больших групп по признаку функции и сложности строения: Жиры, Воска, Фосфатиды, Пигменты (хлорофиллы и каротиноиды), Стероиды.
Жиры - наиболее легко синтезируемая группа липидов. С химической точки зрения - это эфиры жирных кислот и глицерина (дать формулу на доске).
Поскольку жирные кислоты бывают насыщенные и ненасыщенные, то они определяют структуру жира. Поэтому в обыденной практике твердые жиры (включающие насыщенные жирные кислоты) называют жирами, а жидкие жиры с ненасыщенными жирными кислотами - маслами. Твердые жиры - в основном животного происхождения, и маслы - растительного, хотя есть и исключения из правила (рыбий жир и арахисовое масло). Насыщенность жира ненасыщенными жирными кислотами определяют по йодному числу (т.е. по количеству граммов йода, связывающегося 100 г жира).
Основные функции жиров - энергетическая, строительная и запасающая.
Воска - это жироподобные вещества, твердые при комнатной температуре. По химической структуре - это сложные эфиры между жирными кислотами и высокомолекулярными одноатомными спиртами жирного ряда. Основная функция восков - защитная.
Фосфатиды, к которым относятся глицерофосфатиды, лецитины и кефалины - это молекулы сложных эфиров глицерина, жирных кислот и фосфорной кислоты. Эти вещества входят в состав запасных жиров и предохраняют их от прогоркания.
Основная функция фосфатидов - запасающая. Пигменты - это особая группа липидов, имеющая сложное строение, куда входят и азотистые радикалы. Подробно строение пигментов будет изучено в разделе о фотосинтезе. К пигментам относят две группы веществ - хлорофиллы и каротиноиды. Основная функция пигментов - участие в энергетической (световой) фазе фотосинтеза. Стероиды - это производные сложного гетероциклического соединения - циклопентанпергидрофенантрена. Дать формулу. В эту группу соединений входят высокомолекулярные спирты (стеролы) и их сложные эфиры (стериды) Наиболее известный стероид - эргостерол, из которого в промышленности получают витамин Д.Основная функция стероидов - строительная (участвуют в составе мембран).
7. Строение и классификация аминокислот.
Аминокислоты - это мономеры белков, то есть составные компоненты биополимеро, к которым относятся белки.
В состав аминокислот входят углерод, водород, кислород, азот и сера. Общая форму аминокислот - дать формулу.
В природе имеется всего 20 аминокислот, из которых затем в живых организмах синтезируется огромное количество белков.
Все аминокислоты классифицируются на 4 группы:
моноаминомонокарбоновые (глицин, аланин, цистеин, метионин, валин),
моноаминодикарбоновые (аспарагиновая кислота, глутаминовая кислота),
диаминомонокарбоновые (лизин, аргинин),
гетероциклические (триптофан, гистидин).
Аминокислоты обладают амфотерными свойствами, способны к образованию между собой особого типа связей - пептидной и дисульфидной.
количество носителей мутации. Средняя частота неисправленных ошибок - 1 на 10 10
Сходство:
И белок и нуклеиновая кислота - это биополимеры, т.е. биологические макромолекулы. Они состоят из множества (многих тысяч) соединенных друг с другом «звеньев» – мономеров.
Различия:
Мономеры у этих химических соединений разные. Белки состоят из аминокислот, нуклеиновые кислоты состоят из нуклеотидов.
Белки выполняют огромное множество функций, а у нуклеиновых кислот только 2 (передача генетической и реализация генетической информации и синтез белка). Однако, без последовательности нуклеотидов невозможно воспроизвести аминкислотную последовательность в составе белка.
9. Сходства и различия в строении белков и углеводов
БЕЛКИ.
Имеют полимерное строение (сложные полимеры, или поликонденсаты), состоят из множества мономеров. Мономерам белка являются различные аминокислоты (NH2-CHR-COOH).
В составе любой аминокислоты к одному и тому же атому углерода присоединяются две сильно заряженные группы (аминогруппа NH2+ и карбоксильная группа COOH-), благодаря своим свойствам аминокислоты могут принимать участие в сложных химических реакциях, в т.ч. в образовании длинных полимеров. Белки - главный функциональный элемент любого организма. У всех живых существ в формировании белков принимают участие 20 основных аминокислот. Средний размер белка - около 300 аминокислот. Функция конкретного белка определяется последовательностью его аминокислот.
Радикалы:
1 – не несут на себе заряда совсем (углеводородные остатки)
2 – радикалы со слабыми электростатическими зарядами (гидроксильная, карбонильная, тиогруппы)
3 – имеющие сильный положительный заряд (аминогруппа)
4 – сильный отрицательный заряд (карбоксильная, фосфатная группа)
Молекула белка может обладать ОЧЕНЬ сложными хим свойствами и может выполнять ОЧЕНЬ сложные функции.
Благодаря особенностям своего хим строения, белки чрезвычайно разнообразны по своим хим свойствам и выполняемым в организме функциям
Функции:
выполняющиеся только белками:
1. каталитическая (ферментативная);
2. рецепторная;
3. транспортная:
1. пассивный транспорт (по градиенту) - канал;
2. активный транспорт - мембранный насос;
4. двигательная (актин, миозин);
очень важные:
5. регуляторная;
6. сигнальная;
7. защитная;
8. строительная (кератин);
вспомогательные:
9. запасная;
10.энергетическая.
Уровни организации
3) первичная структура – последовательность аминокислот;
4) вторичная структура: - α-спирали;
- β-листы. (многочисленные слабые водорондные связи, за счет которых происходит скручивание во вторичные структуры)
3) третичная структура – трёхмерные молекулы, образующиеся за счёт неиспользованных собственных зарядов. Гидрофобные связи – слабые, но стабильные за счёт количества. S-S связь – прочная, способная связывать молекулы и образовывать третичную структуру;
4) четвертичная структура (молекулярные комплексы). Классический пример - Гемоглобин.(состоит из 2 молекул α-глобина, 2 молекул β -глобина, гемма и иона железа.)
Со вторичной структуры начинается конформация молекул под температурой. Фактором, на неё влияющим, является концентрация различных ионов. Изменив свою конформацию, белок может остаться в стабильном состоянии. Изменение конформации влияет на химические свойства молекулы – способности выполнять необходимую функцию.
В отличие от жиров и углеводов белки обладают огромным структурным разнообразием => биологические функции белков тоже поразительно разнообразны.
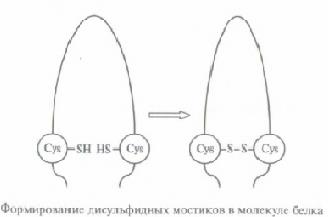
Одним из 20 вариантов аминокислот, используемых в составе белков, является цистин (Cys). В его радикале содержится функциональная группа SH. Если 2 остатка цистина в третичной структуре оказываются поблизости друг от друга, между ними, под действием особого фермента, может возникнуть дисульфидный мостик S-S.Такие мостики играют роль стяжек, стабилизирующих третичную структуру молекулы белка.
Функции конкретной белковой молекулы зависят не только от ее аминокислотной последовательности, но и от ее конформации в данный момент. (например, изменение конформации молекул белка посредством высокой температуры ведет к необратимой инактивации белка (сырое-вареное яйцо)).
Изменяя в своих клетках концентрацию некоторых ионов, организм способен тонко регулировать биологическую активность собственных белков. (кристаллы соли на яичном белке – мутные разводы – временная инактивация белков).
Сходство:
Белки – полимерные соединения. И среди углеводов тоже могут быть полимеры (например, сложные углеводы – крахмал, гликоген, целлюлоза, хитин).
И белки и углеводы выполняют структурную функцию (белки – каркас клетки у животных, углеводы – клеточная стенка)
Углеводы и белки выполняют защитную функцию, у белков она активная (защита организма иммуноглобулинами), а у углеводов пассивная(укрепляет клеточные стенки за счет хитина и целлюлозы).
Различия:
Разные мономеры. У белков – аминокислоты, при том, они могут быть разными, а у углеводов звенья Н-С-ОН. У углеводов строение проще, чем у белков, белки имеют огромное структурное разнообразие.
Углеводы из-за своего однообразного строения могут выполнять только запасную и энергетическую функции, в то время как функции белков поразительно разнообразны.
Белки – сложные полимеры, а углеводы – могут быть полимерами, а могут и не быть.
И белки и углеводы выполняют запасающую функцию (у белков – казеин, у углеводов – крахмал и гликоген)
УГЛЕВОДЫ
Органические вещества, содержащие карбонильную группу и несколько гидроксильных групп. Являются гидрофильными веществами, т.к. много (ОН), многие из них растворимы в воде (сахара).
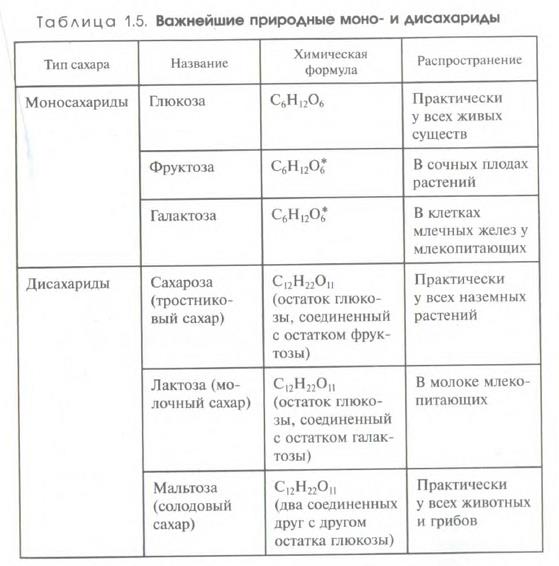
1. Моносахариды (одна небольшая цепочка (3≤n≤7) с несколькими звеньями Н-С-ОН): глюкоза (C6H12O6) – это циклический моносахарид, т.к. его молекулы замыкаются в кольцо через 1 из атомов О2; фруктоза, галактоза (изомеры).
2. Дисахариды (2 кольцевых моносахарида, соединены друг с другом через атом кислорода): сахароза (C12H22O11); (сахароза=глюкоза+фруктоза)
3. Полисахариды : состоят из многочисленных остатков моносахаридов) крахмал, гликоген, целлюлоза, хитин. Из-за крупных размеров своих молекул полисахариды практически нерастворимы в воде и не имеют сладкого вкуса.
Все углеводы устроены более или менее однотипно, следовательно, их функции сравнительно просты и однотипны.
Функции углеводов:
1. Энергетическая. (энергия за счет окисления глюкозы)
C6H12O6 + O2 → CO2 + H2
O + E(АТФ) → свет, тепло, механическая, электрическая,
синтез других связей.
2. Запасная. (запас веществ у многих организмов представлен, в основном, полисахаридами; у животных и грибов полисахарид - гликоген)
3. Строительная (полисахариды составляют основу клеточных стенок)
Конспект урока
Педагогика и дидактика
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру белка. Она уникальна для любого белка и определяет его форму свойства и функции. Эта спираль вторичная структура белка.
Урок 5. Липиды. Состав и строение белков 1.3-1.4
1. Липиды
Липиды. (от греч. lipos жир) обширная группа жироподобных веществ, нерастворимых в воде. Содержание липидов в разных клетках сильно варьирует: от 23 до 5090% в клетках семян некоторых растений и жировой ткани животных.
Липиды присутствуют во всех без исключения клетках, выполняя специфические биологические функции.
Жиры наиболее простые и широко распространенные липиды играют важную роль как источник энергии. При полном расщеплении 1 г жира до конечных продуктов выделяется 38,9 кДж энергии. Жиры состоят из трех остатков высокомолекулярных жирных кислот и трехатомного спирта глицерина (рис. 4). При окислении они дают более чем в два раза больше энергии по сравнению с углеводами.
Жиры являются основной формой запасания энергии в клетке. У позвоночных животных примерно половина энергии, потребляемой клетками в состоянии покоя, образуется за счет окисления жиров.
Жиры могут использоваться также в качестве источника воды (при окислении 1 г жира образуется более 1 г воды). Это особенно ценно для арктических и пустынных животных, обитающих в условиях дефицита свободной воды.
Благодаря низкой теплопроводности липиды выполняют защитные функции, т. е. служат для теплоизоляции организмов. Например, у многих позвоночных животных хорошо выражен подкожный жировой слой, что позволяет им жить в условиях холодного климата, а у китообразных он играет еще и другую роль способствует плавучести.
Липиды выполняют и строительную функцию, так как нерастворимость в воде делает их важнейшими компонентами клеточных мембран.
Многие гормоны (например, коры надпочечников, половые) являются производными липидов. Следовательно, липидам присуща регуляторная функция.
2. Состав и строение белков.
Среди органических веществ белки, или протеины, самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 5080% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (Рис. 5). Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. В состав аминокислот кроме углерода, кислорода, водорода и азота, может входить сера. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой ( NH 2 ) с основными свойствами, другая карбоксильной группой (СООН) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. Через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами.
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации (рис. 6).
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между СО- и NH - rpynna ми разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль вторичная структура белка.
Третичная структура трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация глобула.
Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот. Четвертичная структура характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка (рис. 7).
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам. Нарушение природной структуры белка называют денатурацией (рис. 8). Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов.
При слабом воздействии распадается только четвертичная структура, при более сильном третичная, а затем вторичная, и белок остается в виде полипептидной цепи. Этот процесс частично обратим: если не разрушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенности строения макромолекулы белка определяются его первичной структурой. Кроме простых белков, состоящих только из аминокислот, есть еще и сложные белки, в состав которых могут входить углеводы (гликопротеины), жиры (липопротеины), нуклеиновые кислоты (нуклеопротеины) и др.
Роль белков в жизни клетки огромна. Современная биология показала, что сходство и различие организмов определяется, в конечном счете, набором белков. Чем ближе организмы друг к другу в систематическом положении, тем более сходны их белки.
Карточка у доски:
- Из остатков каких молекул состоят жиры?
- Какова основная функция жиров?
- Сколько энергии выделяется при окислении жира по сравнению с углеводами?
- В чем проявляется строительная функция липидов?
- В чем проявляется регуляторная функция липидов?
- Запишите общую формулу аминокислоты.
- Чем определяется первичная структура белка?
- Чем представлена вторичная структура белка?
- Чем представлена третичная и четвертичная структуры белка?
- Что такое денатурация?
Карточки для письменной работы:
- Определение или сущность термина: 1. Липиды. 2. Жиры. 3. Белки. 4. Аминокислоты. 5. Пептидная связь. 6. Структуры белка. 7. Денатурация.
- Липиды и их значение.
- Строение белков.
- Структуры белковых молекул.
Компьютерное тестирование
**Тест 1 . Из остатков каких молекул состоят жиры?
- Аминокислот.
- Глицерина.
- Высокомолекулярных жирных кислот.
- Нуклеотидов.
Тест 2 . Какова основная функция жиров?
- Строительная.
- Запасающая.
- Энергетическая.
- Хранение генетической информации.
**Тест 3 . Основные функции липидов:
- Строительная. 5. Хранение генетической информации.
- Запасающая. 6. Основной источник энергии для клетки.
- Регуляторная. 7. Источник воды.
- Теплоизоляционная.
Тест 4. Из остатков каких молекул состоят белки?
- Аминокислот.
- Глицерина.
- Жирных кислот.
- Нуклеотидов.
Тест 5
- Основные.
- Кислотные.
Тест 6 . Какие свойства проявляет карбоксильная группа?
- Основные.
- Кислотные.
Тест 7 . Пептидная связь образуется:
- Между карбоксильными группами соседних аминокислот.
- Между аминогруппами соседних аминокислот.
- Между карбоксильной группой одной аминокислоты и аминогруппой другой.
- Между карбоксильной группой одной аминокислоты и радикалом другой.
Тест 8 . Последовательность аминокислот в полипептиде:
- Первичная структура белка.
- Вторичная структура белка.
- Третичная структура белка.
**Тест 9 . Спираль из аминокислот, удерживаемая водородными связями:
- Первичная структура белка.
- Вторичная структура белка.
- Третичная структура белка.
- Четвертичная структура белка.
Тест 10 . Конфигурация полипептида в виде глобулы:
- Первичная структура белка.
- Вторичная структура белка.
- Третичная структура белка.
- Четвертичная структура белка.
А также другие работы, которые могут Вас заинтересовать |
|||
| 72752. | Лингвистические особенности русского палиндрома | 82 KB | |
| История палиндрома уходит в далекую древность. Палиндромические стихи были известны еще в древнем Китае. Многими исследователями отмечаются и заговорно-молитвенные свойства палиндромов, которые позволяли использовать их в качестве заклятий. Так, считалось, что при произнесении «оборачиваемой» фразы... | |||
| 72753. | Лингвистические особенности творчества Гуфа | 80.5 KB | |
| Объект: специфическая форма поэтического творчества Гуфа. Материал для исследования: тексты песен собранные в сети интернет Предмет исследования: языковые особенности текстов Гуфа. Цель: описание лингвистических особенностей текстов Гуфа как представителя рэп-культуры. | |||
| 72754. | История моей семьи в истории России | 48.5 KB | |
| Что каждый из нас знает об истории своей семьи? Мы знаем своих родителей, своих бабушек и дедушек. А вот уже старшие поколения в лучшем случае известны нам по семейным альбомам с фотографиями и письмам. Знать историю семьи – значит знать свою предысторию, свои истоки и корни. | |||
| 72755. | ЛЕКЦИЯ КАК ОДИН ИЗ МЕТОДОВ ОБУЧЕНИЯ | 110 KB | |
| В настоящее время все большее распространение получают модернизированные нетрадиционные лекции. Но в информационном XXI веке когда изменились некоторые принципы и методы обучения возникла необходимость создать определённые алгоритмы образовательного процесса в том числе и лекции. | |||
| 72756. | О чем рассказывают имена и фамилии? | 120 KB | |
| Надо обладать очень большими знаниями, чтобы познать и понять многое из того, что исследовано учеными. Существует большое количество словарей имен и фамилий, написано много книг об истории их происхождения, а тема всегда актуальна. | |||
| 72757. | ИСТОРИЯ ВОЗНИКНОВЕНИЯ СВЕЧИ | 72.5 KB | |
| Так заведено что на новогодние праздники люди часто дарят друг другу декоративные свечи с образом символа года. Во многих семьях эти свечи стоят без надобности пылятся на полочке это в лучшем случае а иной раз и валяются где-то в ящиках комода. | |||
| 72758. | История моей школы в истории Отечества | 470 KB | |
| На старых планах города эта школа именовалась как Александровское шоссе и вела она к Александровскому вокзалу железнодорожной станции. Маленькая деревянная школа не могла принять всех желающих учиться да и обучение оставалось платным. | |||
| 72760. | Почему нельзя пить сырую воду из-под крана? | 53 KB | |
| Говорят, что гномики давно перевелись. Может это и так. Но однажды со мной произошел такой случай. Я играл, бегал, а потом захотел пить. Чайник был горячий, поэтому я взял стакан и налил воды из-под крана. Я уже хотел попить и поднес стакан ко рту. Вдруг кто-то сел ко мне на плечо. От неожиданности я выронил стакан. | |||



