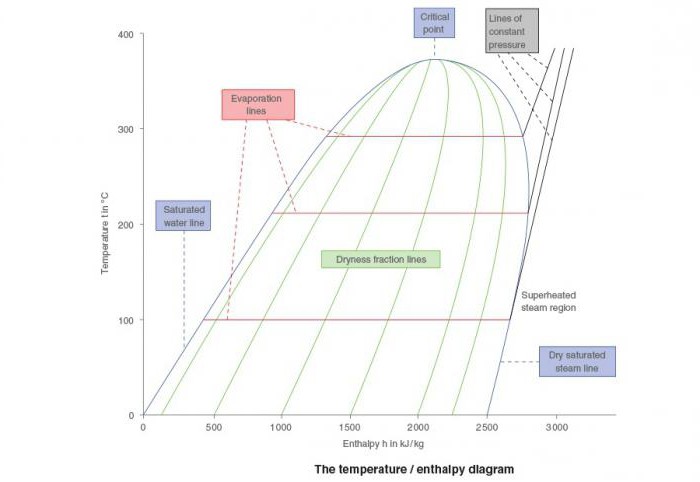
Когда пар насыщенный. Насыщенный пар и его свойства
После закипания температура воды перестает расти и остается неизменной до полного испарения. Парообразование - это процесс перехода из жидкого состояния в пар, который имеет тот же температурный показатель, что и кипящая жидкость. Это испарение получило название насыщенный пар. Когда вся вода испаряется, любое последующее добавление тепла повышает температуру. Нагретый пар за уровнем насыщенного называется перегретым. В промышленности обычно используется насыщенный пар для отопления, приготовления пищи, сушки или других процедур. Перегретый используется исключительно для турбин. Различные типы пара имеют разные энергии обменного потенциала и это оправдывает их применение в совершенно различных целях.
Пар как одно из трех физических состояний
Лучше понять свойства пара может помочь понимание общего молекулярного и атомарного строения вещества, а также применение этого знания касательно льда, воды и пара. Молекула - это наименьшая единица любого элемента или соединения. Она, в свою очередь, состоит из еще более мелких частиц, называемых атомами, которые определяют базовые элементы, такие как водород и кислород. Конкретные комбинации этих атомарных элементов обеспечивают соединение веществ. Одно из таких соединений представлено химической формулой Н 2 О, молекулы которого состоят из 2 атомов водорода и 1 атома кислорода. Углерода имеется также в изобилии, это ключевой компонент всех органических веществ. Большинство минеральных веществ могут существовать в трех физических состояниях (твердое тело, жидкость и пар), которые называются фазами.
Процесс образования пара
Когда температура воды приближается к точке кипения, некоторые молекулы получают достаточное количество кинетической энергии для достижения скоростей, которые позволяют им на мгновение отделиться от жидкости в пространстве над поверхностью, прежде чем вернуться. Дальнейшее нагревание вызывает большее возбуждение и число молекул, желающих покинуть жидкость, увеличивается. При атмосферном давлении температура насыщения составляет 100 °С. Пар с температурой кипения при таком давлении носит название сухой насыщенный пар. Как фазовый переход от льда к воде, процесс испарения является также обратимым (конденсация). Критическая точка - это наибольшая температура, при которой вода может находиться в жидком состоянии. Выше этой точки пар может рассматриваться как газ. Газообразное состояние является подобием диффузного, в котором молекулы имеют почти неограниченную возможность движения.
Взаимосвязь переменных
При заданной температуре существует определенное давление пара, которое существует в равновесии с жидкой водой. Если этот показатель растет, пар перегревается и называется сухим. Существует взаимосвязь между давлением и температурой: зная одно значение, можно определить другое. Состояние пара определяется тремя переменными: давлением, температурой и объемом. Сухой насыщенный пар - это состояние, когда пар и вода могут присутствовать одновременно. Иными словами, это происходит тогда, когда скорость парообразования равна скорости конденсации.
Насыщенный пар и его свойства
При обсуждении свойств насыщенного пара его часто сравнивают с иде-аль-ным газом. Есть ли у них что-то общее или это простое заблуждение? Во-первых, при неизменном уровне тем-пе-ра-ту-ры плот-ность не находится в за-ви-симости от объ-е-ма. Визуально это можно себе представить следующим образом: нужно визуально уменьшить объем емкости с паром, не изменяя при этом температурные показатели. Число конденсируемых мо-ле-кул будет пре-восходить число испаряющихся, а пар будет возвращаться в со-сто-я-ние баланса. В результате плот-ность будет неизменным параметром. Во-вторых, такие характеристики, как дав-ле-ние и объ-е-м, не зависят друг от друга. В-третьих, учитывая неизменность объ-е-мных характеристик, плот-ность молекул возрастает, когда растет тем-пе-ра-ту-ра, и становится меньше, когда она понижается. На самом деле, при нагревании вода начинает испаряться быстрее. Баланс в этом случае будет нарушен и не будет восстановлен до тех пор, пока плот-ность пара не вернется на прежние позиции. При конденсации, наоборот, плотность насыщенного пара будет уменьшаться. В отличие от идеального газа, насыщенный пар нельзя назвать замкнутой системой, так как он постоянно контактирует с водой.

Преимущества в сфере отопления
Насыщенным называется чистый пар в непосредственном контакте с жидкой водой. Он обладает многими характеристиками, которые делают его отличным источником тепловой энергии, особенно это касается высоких температур (выше 100 °C). Некоторые из них:

Различные виды пара
Пар - это газообразная фаза воды. Он использует тепло во время своего образования и выделяет большое количество тепла после этого. Следовательно, он
может быть использован в качестве рабочего вещества для тепловых двигателей. Известны следующие состояния: влажный насыщенный, сухой насыщенный и перегретый. Насыщенный пар предпочтительнее перегретого пара в качестве теплоносителя в теплообменниках. Когда он выбрасывается в атмосферу из труб, часть его конденсируется, образуются облака белого влажного испарения, содержащего мельчайшие капельки воды. Перегретый пар не будет подвержен конденсации, даже при вступлении в непосредственный контакт с атмосферой. В перегретом состоянии он будет иметь большую теплоотдачу за счет ускорения движения молекул и меньшей плотности. Наличие влаги вызывает осаждение, коррозию и снижению продолжительности службы котлов или другого теплообменного оборудования. Следовательно, сухой пар является предпочтительным, поскольку он вырабатывает больше энергии и не вызывает коррозии.

Сухой и насыщенный: в чем противоречие
Многие путаются с терминами "сухой" и "насыщенный". Как может быть нечто одновременно и тем и другим? Ответ кроется в терминологии, которую мы используем. Термин «сухой» связывают с отсутствием влаги, то есть «не мокрый». «Насыщенный» означает "замоченный", "промокший", "затопленный", "заваленный" и так далее. Все это, казалось бы, подтверждает противоречие. Однако в паровой инженерии термин «насыщенный» имеет другое значение и в данном контексте означает состояние, при котором происходит кипение. Таким образом, температура, при которой происходит кипение, известна технически как температуры насыщения. Сухой пар в данном контексте не имеет в себе влаги. Если понаблюдать за кипящим чайником, то можно увидеть выходящее из носика чайника белое испарение. На самом деле, это смесь сухого бесцветного пара и влажного пара, содержащего в себе капельки воды, которые отражают свет и окрашиваются в белый цвет. Поэтому термин «сухой насыщенный пар» означает, что пар обезвожен и не перегрет. Свободное от частиц жидкости, это вещество в газообразном состоянии, которое не следуют общим газовым законам.
Тема 2. ФАЗОВЫЕ ПЕРЕХОДЫ.
Фазовый переход (фазовое превращение) – это переход вещества из одной фазы в другую при изменении внешних русловий (например, температуры, давления, магнитного и электрического полей и т.д.), сопровождающееся изменением физических свойств и параметров вещества.
Значение температуры, давления или какой-либо другой физической величины, при котором происходит Фазовый переход, называют точкой перехода. Различают Фазовый переход двух родов.
ФАЗОВЫЕ ПЕРЕХОДЫ ПЕРВОГО РОДА
При фазовом переходе первого рода скачком меняются такие термодинамические
характеристики вещества, как плотность, концентрация компонент, удельный объём, количество запасённой внутренней энергии, т.е. выделяется или поглощается определённое количество теплоты, носящее название теплоты перехода. Причем имеется в виду скачкообразное изменение этих величин не во времени, а при изменении температуры, давления и т. п. Наиболее распространённые примеры фазовых переходов первого рода:
- плавление и кристаллизация
- испарение и конденсация
- сублимация и десублимация
ФАЗОВЫЕ ПЕРЕХОДЫ ВТОРОГО РОДА
При фазовом переходе второго рода плотность и внутренняя энергия не меняются, так что невооружённым глазом такой фазовый переход может быть незаметен. Скачок же испытывают их производные по температуре и давлению: теплоёмкость, коэффициент теплового расширения, различные восприимчивости и т. д. Т.е. фазовые переходы второго рода сопровождаются изменением симметрии строения вещества, а не выделением или поглощением энергии (теплоты). Наиболее распространённые примеры фазовых переходов второго рода:
- прохождение системы через критическую точку
- переход парамагнетик-ферромагнетик
- переход металлов и сплавов в состояние сверхпроводимости
- переход жидкого гелия в сверхтекучее состояние
- переход аморфных материалов в стеклообразное состояние
Современная физика исследует также системы, обладающие фазовыми переходами третьего или более высокого рода. В последнее время широкое распространение получило понятие квантовый фазовый переход, т.е. фазовый переход, управляемый не классическими тепловыми флуктуациями, а квантовыми, которые существуют даже при абсолютном нуле температур, где классический фазовый переход не может реализоваться вследствие теоремы Нернста .
Рассмотрим более подробно интересующие нас явления, связанные с фазовыми переходами первого рода.
ИСПАРЕНИЕ, КОНДЕНСАЦИЯ, КИПЕНИЕ.
НАСЫЩЕННЫЕ И НЕНАСЫЩЕННЫЕ ПАРЫ.
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. Переходы из одного агрегатного состояния во второе являются фазовыми переходами I рода.
Испарение и конденсация являются фазовыми переходами между жидкой и газообразной фазой вещества..
Все реальные газы (кислород, азот, водород и т. д.) при определенных условиях способны превращаться в жидкость. Однако такое превращение может происходить только при температурах ниже определенной, так называемой критической температуры T кр. Например, для воды критическая температура равна 647,3 К, для азота 126 К, для кислорода 154,3 К. При комнатной температуре (≈ 300 К) вода может находиться и в жидком, и в газообразном состояниях, а азот и кислород существуют только в виде газов.
Испарением называется фазовый переход из жидкого состояния в газообразное. С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости (если нет подвода энергии от окружающих тел).
Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия , когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, т. е. когда скорости процессов испарения и конденсации одинаковы. Такую систему называют двухфазной . Пар, находящийся в равновесии со своей жидкостью, называют насыщенным .
Число молекул, вылетающих с единицы площади поверхности жидкости за одну секунду, зависит от температуры жидкости. Число молекул, возвращающихся из пара в жидкость, зависит от концентрации молекул пара и от средней скорости их теплового движения, которая определяется температурой пара. Отсюда следует, что для данного вещества концентрация молекул пара при равновесии жидкости и ее пара определяется их равновесной температурой. Установление динамического равновесия между процессами испарения и конденсации при повышении температуры происходит при более высоких концентрациях молекул пара. Так как давление газа (пара) определяется его концентрацией и температурой, то можно сделать вывод: давление насыщенного пара p 0 данного вещества зависит только от его температуры и не зависит от объема . Поэтому изотермы реальных газов на плоскости (p , V ) содержат горизонтальные участки, соответствующие двухфазной системе (рис. 3.4.1).
При повышении температуры давление насыщенного пара и его плотность возрастают, а плотность жидкости уменьшается из-за теплового расширения. При температуре, равной критической температуре T кр для данного вещества, плотности пара и жидкости становятся одинаковыми. При T > T кр исчезают физические различия между жидкостью и ее насыщенным паром.
Если изотермически сжимать ненасыщенный пар при T < T кр, то его давление будет возрастать, пока не станет равным давлению насыщенного пара. При дальнейшем уменьшении объема на дне сосуда образуется жидкость и устанавливается динамическое равновесие между жидкостью и ее насыщенным паром. С уменьшением объема все большая часть пара конденсируется, а его давление остается неизменным (горизонтальный участок на изотерме). Когда весь пар превращается в жидкость, давление резко возрастает при дальнейшем уменьшении объема вследствие малой сжимаемости жидкости.
Из газообразного состояния в жидкое можно перейти, минуя двухфазную область. Для этого нужно совершить процесс в обход критической точки K . Один из возможных процессов такого рода показан на рис.1 ломаной линией ABC .
В атмосферном воздухе всегда присутствуют пары воды при некотором парциальном давлении p , которое, как правило, меньше давления насыщенного пара p 0 . Отношение p / p 0 , выраженное в процентах, называется относительной влажностью воздуха.
| |
Ненасыщенный пар можно теоретически описывать с помощью уравнения состояния идеального газа при обычных для реальных газов ограничениях: давление пара должно быть не слишком велико (практически p ≤ (10 6 –10 7) Па), а его температура выше некоторого определенного для каждого вещества значения. К насыщенному пару также можно приближенно применять законы идеального газа при условии, что для каждой температуры T давление p 0 насыщенного пара определяется по кривой равновесия p 0 (T ) для данного вещества.
Давление p 0 насыщенного пара очень быстро возрастает с ростом температуры T . Зависимость p 0 (T ) нельзя получить из законов идеального газа. Давление газа при постоянной концентрации молекул растет прямо пропорционально температуре. В насыщенном паре при повышении температуры возрастает не только средняя кинетическая энергия движения молекул, но и их концентрация. Поэтому давление насыщенного пара при повышении температуры возрастает быстрее, чем давление идеального газа при постоянной концентрации молекул.
Испарение может происходить не только с поверхности, но и в объеме жидкости. В жидкости всегда имеются мельчайшие пузырьки газа. Если давление насыщенного пара жидкости равно внешнему давлению (т. е. давлению газа в пузырьках) или превышает его, жидкость будет испаряться внутрь пузырьков. Пузырьки, наполненные паром, расширяются и всплывают на поверхность. Этот процесс называется кипением . Таким образом, кипение жидкости начинается при такой температуре, при которой давление ее насыщенных паров становится равным внешнему давлению .
В частности, при нормальном атмосферном давлении вода кипит при температуре 100 °С. Это значит, что при такой температуре давление насыщенных паров воды равно 1 атм. При подъеме в горы атмосферное давление уменьшается, и поэтому температура кипения воды понижается (приблизительно на 1 °С на каждые 300 метров высоты). На высоте 7 км давление составляет примерно 0,4 атм, и температура кипения понижается до 70 °С.
В герметически закрытом сосуде жидкость кипеть не может, т. к. при каждом значении температуры устанавливается равновесие между жидкостью и ее насыщенным паром. По кривой равновесия p 0 (T ) можно определять температуру кипения жидкости при различных давлениях.
Изображенная на рис.1 картина изотерм реального газа описывает процессы испарения и конденсации, т. е. фазовый переход между газообразной и жидкой фазами вещества. На самом деле эта картина является неполной, т. к. из газообразного и жидкого любое вещество может перейти в твердое состояние. При заданной температуре T термодинамическое равновесие между двумя фазами одного и того же вещества возможно лишь при определенном значении давления в системе. Зависимость равновесного давления от температуры называется кривой фазового равновесия . Примером может служить кривая равновесия p 0 (T )насыщенного пара и жидкости. Если кривые равновесия между различными фазами данного вещества построить на плоскости (p , T ), то они разбивают эту плоскость на отдельные области, в которых вещество существует в однородном агрегатном состоянии – твердом, жидком или газообразном (рис. 2). Изображенные в координатной системе (p , T ) кривые равновесия называются фазовой диаграммой .
Кривая 0T , соответствующая равновесию между твердой и газообразной фазами, называется кривой сублимации . Кривая TK равновесия между жидкостью и паром называется кривой испарения , она обрывается в критической точке K . Кривая TM равновесия между твердым телом и жидкостью называется кривой плавления .
Кривые равновесия сходятся в точке T , в которой могут сосуществовать в равновесии все три фазы. Эта точка называется тройной точкой .
Для многих веществ давление p тр в тройной точке меньше 1 атм ≈ 10 5 Па. Такие вещества при нагревании при атмосферном давлении плавятся. Например, тройная точка воды (рис. 3) имеет координаты T тр = 273,16 К, p тр = 6,02·10 2 Па и используется в качестве опорной для калибровки абсолютной температурной шкалы Кельвина.
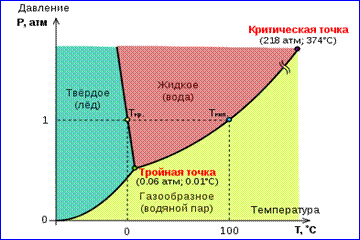 Существуют, однако, и такие Рис. 3 Фазовая диаграмма воды
Существуют, однако, и такие Рис. 3 Фазовая диаграмма воды
вещества, у которых p тр
превышает 1 атм. Так для
углекислоты (CO 2) давление
p тр = 5,11 атм и температура
T тр = 216,5 К. Поэтому при атмосферном
давлении твердая углекислота может
существовать только при низкой температуре, а в жидком состоянии при p = 1 атм она вообще не существует. В твердом состоянии в равновесии со своим паром при атмосферном давлении углекислота находится при температуре 173 К или –80 °С. Это широко применяемый «сухой лед», который никогда не плавится, а только испаряется (сублимирует).
Процессы испарения и конденсации идут непрерывно и параллельно друг другу.
В открытом сосуде количество жидкости со временем уменьшается, т.к. испарение преобладает над конденсацией.
Пар, который находится над поверхностью жидкости, когда испарение преобладает над конденсацией или пар при отсутствии жидкости, называется ненасыщенным.
В герметически закрытом сосуде уровень жидкости со временем не изменяется, т.к. испарение и конденсация компенсируют друг друга: сколько молекул вылетает из жидкости, столько же их за тоже время возвращается в неё, наступает динамическое (подвижное) равновесие между паром и его жидкостью.
Пар, который находится в динамическом равновесии со своей жидкостью, называется насыщенным.
При данной температуре насыщенный пар какой-либо жидкости имеет наибольшую плотность ( ) и создаёт максимальное давление ( ), которое может иметь пар этой жидкости при этой температуре.
Давление и плотность насыщенного пара при одной и той же температуре зависит от рода вещества: большее давление создаёт насыщенный пар той жидкости, которая быстрее испаряется. Например, и
Свойства ненасыщенных паров: Ненасыщенные пары подчиняются газовым законам Бойля – Мариотта, Гей-Люссака, Шарля, к ним можно применять уравнение состояния идеального газа.
Свойства насыщенных паров: 1. При неизменном объёме с возрастанием температуры давление насыщенного пара увеличивается, но не прямо пропорционально (закон Шарля не выполняется), давление растёт быстрее, чем у идеального газа. , при возрастании температуры () , увеличивается масса пара, а поэтому возрастает концентрация молекул пара () и давление насыщенного пара растает по двум причинам (
3 1 – ненасыщенный пар (идеальный газ);
2 2 – насыщенный пар; 3 – ненасыщенный пар,
1 полученный из насыщенного пара в том же
Объёме при нагревании.
2. Давление насыщенного пара при неизменной температуре не зависит от занимаемого им объёма.
С увеличением объёма масса пара увеличивается, а масса жидкости уменьшается (часть жидкости переходит в пар), при уменьшении объёма пара становится меньше, а жидкости больше (часть пара переходит в жидкость), плотность же и концентрация молекул насыщенного пара остаются постоянными, следовательно, и давление остаётся постоянным ().
жидкость
(насыщ. пар + жидкость )
Ненасыщ. пар
Насыщенные пары не подчиняются газовым законам Бойля – Мариотта, Гей-Люссака, Шарля, т.к. масса пара в процессах не остаётся постоянной, а все газовые законы получены для неизменной массы. К насыщенному пару можно применять уравнение состояния идеального газа.
Итак, насыщенный пар можно перевести в ненасыщенный пар, либо нагревая его при постоянном объёме, либо увеличивая его объём при постоянной температуре. Ненасыщенный пар можно перевести в насыщенный пар, либо охлаждая его при постоянном объёме, либо сжимая его при постоянной температуре.
Критическое состояние
Наличие свободной поверхности у жидкости даёт возможность указать, где находится жидкая фаза вещества, а где газообразная. Резкое различие между жидкостью и её паром объясняется тем, что плотность жидкости во много раз больше, чем у пара. Если нагревать жидкость в герметически закрытом сосуде, то вследствие расширения её плотность будет уменьшаться, а плотность пара над ней увеличиваться. Это означает, что различие между жидкостью и её насыщенным паром сглаживается и при достаточно высокой температуре исчезает совсем. Температура, при которой исчезают различия в физических свойствах между жидкостью и её насыщенным паром, и их плотности становятся одинаковыми, называется критической температурой.
Критическая точка
Для образования жидкости из газа средняя потенциальная энергия притяжения молекул должна превышать их среднюю кинетическую энергию.
Критическая температура – максимальная температура, при которой пар превращается в жидкость. Критическая температура зависит от потенциальной энергии взаимодействия молекул и поэтому различна для разных газов. Из-за сильного взаимодействия молекул воды водяной пар можно превратить в воду даже при температуре . В то же время сжижение азота происходит лишь при температуре, меньшей =-147˚ , т.к. молекулы азота слабо взаимодействуют между собой.
Другим макроскопическим параметром, влияющим на переход пар - жидкость, является давление. С ростом внешнего давления при сжатии газа уменьшается среднее расстояние между частицами, возрастает сила притяжения между ними и соответственно средняя потенциальная энергия их взаимодействия.
Давление насыщенного пара при его критической температуре называется критическим . Это наибольшее возможное давление насыщенного пара данного вещества.
Состояние вещества с критическими параметрами называется критическим (критическая точка). У каждого вещества свои критические температура и давление.
В критическом состоянии обращаются в нуль удельная теплота парообразования и коэффициент поверхностного натяжения жидкости. При температурах выше критической, даже при очень больших давлениях невозможно превращение газа в жидкость, т.е. выше критической температуры жидкость не может существовать. При сверхкритических температурах возможно только парообразное состояние вещества.
Сжижение газов возможно лишь при температурах ниже критической температуры. Для сжижения газы охлаждают до критической температуры, например, при адиабатном расширении, а затем изотермически сжимают.
Кипение
Внешне явление выглядит так: со всего объёма жидкости к поверхности поднимаются быстро растущие пузырьки, на поверхности они лопаются, и пар выбрасывается в окружающую среду.
МКТ объясняет кипение так: в жидкости всегда есть пузырьки воздуха, в них из жидкости происходит испарение. Замкнутый объём пузырьков оказывается заполненным не только воздухом, но и насыщенным паром. Давление насыщенного пара в них при нагревании жидкости растёт быстрее, чем давление воздуха. Когда в достаточно нагретой жидкости давление насыщенного пара в пузырьках становится больше внешнего давления, они увеличиваются в объёме, и выталкивающая сила, превосходящая их силу тяжести, поднимает пузырьки к поверхности. Всплывшие пузырьки начинают лопаться, когда при определённой температуре давление насыщенного пара в них превосходит давление над жидкостью. Температура жидкости, при которой давление её насыщенного пара в пузырьках равно или превышает внешнее давление на жидкость, называется температурой кипения.
Температура кипения различных жидкостей различна , т.к. давление насыщенного пара в их пузырьках сравнивается с одним и тем же внешним давлением при разных температурах. Например, давление насыщенного пара в пузырьках равно нормальному атмосферному давлению у воды при 100˚С, у ртути при 357˚С, у спирта при 78˚С, у эфира при 35˚С.
Температура кипения в процессе кипения остаётся постоянной, т.к. всё тепло, которое подводится к нагреваемой жидкости, тратится на парообразование.
Температура кипения зависит от внешнего давления на жидкость: с увеличением давления температура повышается; с уменьшением давления температура понижается. Например, на высоте 5км над уровнем моря, где давление в 2 раза ниже атмосферного, температура кипения воды 83˚С, в котлах паровых машин, где давление пара 15 атм. (), температура воды около 200˚С.
Влажность воздуха
В воздухе всегда есть водяной пар, поэтому можно говорить о влажности воздуха, которая характеризуется следующими величинами:
1.Абсолютная влажность – это плотность водяного пара, находящегося в воздухе ( или давление, которое этот пар создаёт ( .
Абсолютная влажность не даёт представление о степени насыщения воздуха водяными парами. Одно и то же количество водяного пара при разной температуре создаёт разное ощущение влажности.
2.Относительная влажность - это отношение плотности (давления) водяного пара, содержащегося в воздухе при данной температуре, к плотности (давлению) насыщенного пара при той же температуре : или
– абсолютная влажность при данной температуре; - плотность, давление насыщенного пара при той же температуре. Плотность и давление насыщенного водяного пара при любой температуре можно найти в таблице. Из таблицы видно, чем выше температура воздуха, тем больше должны быть плотность и давление водяного пара в воздухе, чтобы он был насыщенным.
Зная относительную влажность, можно понять, на сколько процентов водяной пар в воздухе при данной температуре далёк от насыщения. Если пар в воздухе насыщенный, то . Если , то до состояния насыщения в воздухе не хватает пара.
О том, что пар в воздухе становится насыщенным, судят по появлению влаги в виде тумана, росы. Температура, при которой водяной пар в воздухе становится насыщенным, называется точкой росы.
Пар в воздухе можно сделать насыщенным, если добавить пары за счёт дополнительного испарения жидкости, не меняя температуры воздуха, или при имеющемся количестве пара в воздухе понизить его температуру.
Нормальная относительная влажность, наиболее благоприятная для человека 40 - 60%. Большое значение имеет знание влажности в метеорологии для предсказания погоды. В ткацком, кондитерском производстве для нормального течения процесса необходима определённая влажность. Хранение произведений искусства и книг требует поддержания влажности воздуха на необходимом уровне.
Приборы для определения влажности:
1. Конденсационный гигрометр (позволяет определить точку росы).
2. Волосной гигрометр (принцип действия основан на зависимости длины обезжиренного волоса от влажности) измеряет относительную влажность в процентах.
3. Психрометр состоит из двух термометров сухого и увлажнённого. Резервуар увлажнённого термометра обмотан тканью, опущенной в воду. За счёт испарения с ткани температура увлажнённого ниже, чем сухого. Разность показаний термометров зависит от влажности окружающего воздуха: чем суше воздух, тем интенсивнее испарение с ткани, тем больше разность показаний термометров и наоборот. Если влажность воздуха 100%, то показания термометров одинаковые, т.е. разность показаний 0. Для определения влажности с помощью психрометра используют психрометрическую таблицу.
Плавление и кристаллизация
При плавлении твёрдого тела увеличивается расстояние между частицами, образующими кристаллическую решётку, и происходит разрушение самой решётки. На процесс плавления необходимо затрачивать энергию. При нагревании твёрдого тела возрастает кинетическая энергия колеблющихся молекул и соответственно амплитуда их колебаний. При определённой температуре, называемой температурой плавления, нарушается порядок в расположении частиц в кристаллах, кристаллы теряют свою форму. Вещество плавится, переходя из твёрдого состояния в жидкое состояние.
При кристаллизации происходит сближение молекул, которые образуют кристаллическую решётку. Кристаллизация может происходить только тогда, когда жидкость отдаёт энергию. При охлаждении расплавленного вещества средняя кинетическая энергия и скорость молекул уменьшаются. Силы притяжения могут удерживать частицы около положения равновесия. При определённой температуре, называемой температурой отвердевания (кристаллизации), все молекулы оказываются в положении устойчивого равновесия, их расположение становится упорядоченным – образуется кристалл.
Плавление твёрдого тела происходит при той же температуре, при которой это вещество отвердевает
Каждое вещество имеет свою температуру плавления. Например, температуры плавления у гелия -269,6˚С, у ртути -38,9˚С, у меди 1083˚С.
Во время процесса плавления температура остаётся постоянной. Подводимое извне количество теплоты идёт на разрушение кристаллической решётки.
Во время процесса отвердевания, не смотря на то, что тепло отводится, температура не меняется. Выделяющаяся при кристаллизации энергия расходуется на поддержание постоянной температуры.
Пока всё вещество не расплавится или всё вещество не отвердеет, т.е. пока существуют совместно твёрдая и жидкая фазы вещества, температура не изменяется.
Тв.+жид. жид.+тв.
, где – количество теплоты, - количество теплоты, необходимое для расплавления вещества выделяемое при кристаллизации вещества массой массой
- удельная теплота плавления – количество теплоты, необходимое для плавления вещества массой 1кг при температуре плавления.
Какое количество теплоты затрачивается при плавлении определённой массы вещества, такое же количество теплоты выделяется при кристаллизации этой массы.
Называется также удельной теплотой кристаллизации .
При температуре плавления внутренняя энергия вещества в жидком состоянии больше внутренней энергии такой же массы вещества в твёрдом состоянии.
У большого числа веществ объём при плавлении увеличивается, а плотность уменьшается. При отвердевании наоборот, объём уменьшается, а плотность увеличивается. Например, кристаллики твёрдого нафталина тонут в жидком нафталине.
Некоторые вещества, например, висмут, лёд, галлий, чугун и др. при плавлении сжимаются, а при отвердевании расширяются. Эти отклонения от общего правила объясняются особенностями строения кристаллических решёток. Поэтому вода оказывается плотнее льда, лёд плавает в воде. Расширение воды при замерзании ведёт к разрушению горных пород.
Изменение объёма металлов при плавлении и отвердевании имеет существенное значение в литейном деле.
Опыт показывает, что изменение внешнего давления на твёрдое вещество отражается на температуре плавления этого вещества . Для тех веществ, которые при плавлении расширяются, увеличение внешнего давления приводит к повышению температуры плавления, т.к. затрудняет процесс плавления. Если же вещества при плавлении сжимаются, то для них увеличение внешнего давления ведёт к понижению температуры плавления, т.к. помогает процессу плавления. Только очень большое увеличение давления заметно изменяет температуру плавления. Например, чтобы понизить температуру плавления льда на 1˚С, давление нужно повысить на 130 атм. Температуру плавления вещества при нормальном атмосферном давлении называют точкой плавления вещества.
Если открытый стакан с водой оставить на долгое время, то в конце концов вода полностью улетучится. Точнее испарится. Что такое испарение и почему оно происходит?
2.7.1 Испарение и конденсация
При данной температуре молекулы жидкости обладают разными скоростями. Скорости большинства молекул находятся вблизи некоторого среднего значения (характерного для этой температуры). Но попадаются молекулы, скорости которых значительно отличаются от средней как в меньшую, так и б´ольшую сторону.
На рис. 2.16 изображён примерный график распределения молекул жидкости по скоростям. Голубым фоном показано то самое большинство молекул, скорости которых группируются около среднего значения. Красный ¾хвост¿ графика это небольшое число ¾быстрых¿ молекул, скорости которых существенно превышают среднюю скорость основной массы молекул жидкости.
Число молекул
Быстрые молекулы
Скорость молекул
Рис. 2.16. Распределение молекул по скоростям
Когда такая весьма быстрая молекула окажется на свободной поверхности жидкости (т. е. на границе раздела жидкости и воздуха), кинетической энергии этой молекулы может хватить на то, чтобы преодолеть силы притяжения остальных молекул и вылететь из жидкости. Данный процесс и есть испарение, а молекулы, покинувшие жидкость, образуют пар.
Итак, испарение это процесс превращения жидкости в пар, происходящий на свободной поверхности жидкости7 .
Может случиться, что через некоторое время молекула пара вернётся обратно в жидкость.
Процесс перехода молекул пара в жидкость называется конденсацией. Конденсация пара процесс, обратный испарению жидкости.
2.7.2 Динамическое равновесие
А что будет, если сосуд с жидкостью герметично закрыть? Плотность пара над поверхностью жидкости начнёт увеличиваться; частицы пара будут всё сильнее мешать другим молекулам жидкости вылетать наружу, и скорость испарения станет уменьшаться. Одновременно начнёт
7 При особых условиях превращение жидкости в пар может происходить по всему объёму жидкости. Данный процесс вам хорошо известен это кипение.
p н = н RT:
увеличиваться скорость конденсации, так как с возрастанием концентрации пара число молекул, возвращающихся в жидкость, будет становиться всё больше.
Наконец, в какой-то момент скорость конденсации окажется равна скорости испарения. Наступит динамическое равновесие между жидкостью и паром: за единицу времени из жидкости будет вылетать столько же молекул, сколько возвращается в неё из пара. Начиная с этого момента количество жидкости перестанет убывать, а количество пара увеличиваться; пар достигнет ¾насыщения¿.
Насыщенный пар это пар, который находится в состоянии динамического равновесия со своей жидкостью. Пар, не достигший состояния динамического равновесия с жидкостью, называется ненасыщенным.
Давление и плотность насыщенного пара обозначаются pн ин . Очевидно, pн ин это максимальные давление и плотность, которые может иметь пар при данной температуре. Иными словами, давление и плотность насыщенного пара всегда превышают давление и плотность ненасыщенного пара.
2.7.3 Свойства насыщенного пара
Оказывается, что состояние насыщенного пара (а ненасыщенного тем более) можно приближённо описывать уравнением состояния идеального газа (уравнением Менделеева Клапейрона). В частности, имеем приближённое соотношение между давлением насыщенного пара и его плотностью:
Это весьма удивительный факт, подтверждаемый экспериментом. Ведь по своим свойствам насыщенный пар существенно отличается от идеального газа. Перечислим важнейшие из этих отличий.
1. При неизменной температуре плотность насыщенного пара не зависит от его объёма.
Если, например, насыщенный пар изотермически сжимать, то его плотность в первый момент возрастёт, скорость конденсации превысит скорость испарения, и часть пара конденсируется в жидкость до тех пор, пока вновь не наступит динамическое равновесие, в котором плотность пара вернётся к своему прежнему значению.
Аналогично, при изотермическом расширении насыщенного пара его плотность в первый момент уменьшится (пар станет ненасыщенным), скорость испарения превысит скорость конденсации, и жидкость будет дополнительно испаряться до тех пор, пока опять не установится динамическое равновесие т. е. пока пар снова не станет насыщенным с прежним значением плотности.
2. Давление насыщенного пара не зависит от его объёма.
Это следует из того, что плотность насыщенного пара не зависит от объёма, а давление однозначно связано с плотностью уравнением (2.6 ).
Как видим, закон Бойля Мариотта, справедливый для идеальных газов, для насыщенного пара не выполняется. Это и не удивительно ведь он получен из уравнения Менделеева Клапейрона в предположении, что масса газа остаётся постоянной.
3. При неизменном объёме плотность насыщенного пара растёт с повышением температуры и уменьшается с понижением температуры.
Действительно, при увеличении температуры возрастает скорость испарения жидкости. Динамическое равновесие в первый момент нарушается, и происходит дополнительное
испарение некоторой части жидкости. Пара будет прибавляться до тех пор, пока динамическое равновесие вновь не восстановится.
Точно так же при понижении температуры скорость испарения жидкости становится меньше, и часть пара конденсируется до тех пор, пока не восстановится динамическое равновесие но уже с меньшим количеством пара.
Таким образом, при изохорном нагревании или охлаждении насыщенного пара его масса меняется, поэтому закон Шарля в данном случае не работает. Зависимость давления насыщенного пара от температуры уже не будет линейной функцией.
4. Давление насыщенного пара растёт с температурой быстрее, чем по линейному закону.
В самом деле, с увеличением температуры возрастает плотность насыщенного пара, а согласно уравнению (2.6 ) давление пропорционально произведению плотности на температуру.
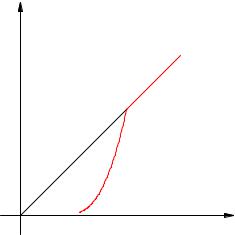
Зависимость давления насыщенного пара от температуры является экспоненциальной (рис. 2.17 ). Она представлена участком 1–2 графика. Эту зависимость нельзя вывести из законов идеального газа.
изохора пара
Рис. 2.17. Зависимость давления пара от температуры
В точке 2 вся жидкость испаряется; при дальнейшем повышении температуры пар становится ненасыщенным, и его давление растёт линейно по закону Шарля (участок 2–3).
Вспомним, что линейный рост давления идеального газа вызван увеличением интенсивности ударов молекул о стенки сосуда. В случае нагревания насыщенного пара молекулы начинают бить не только сильнее, но и чаще ведь пара становится больше. Одновременным действием этих двух факторов и вызван экспоненциальный рост давления насыщенного пара.
2.7.4 Влажность воздуха
Абсолютная влажность это парциальное давление водяного пара, находящегося в воздухе (т. е. давление, которое водяной пар оказывал бы сам по себе, в отсутствие других газов). Иногда абсолютной влажностью называют также плотность водяного пара в воздухе.
Относительная влажность воздуха " это отношение парциального давления водяного пара в нём к давлению насыщенного водяного пара при той же температуре. Как правило, это
отношение выражают в процентах:
" = p 100%: pн
Из уравнения Менделеева-Клапейрона (2.6 ) следует, что отношение давлений пара равно отношению плотностей. Так как само уравнение (2.6 ), напомним, описывает насыщенный пар лишь приближённо, мы имеем приближённое соотношение:
" = 100%:н
Одним из приборов, измеряющих влажность воздуха, является психрометр. Он включает в себя два термометра, резервуар одного из которых завёрнут в мокрую ткань. Чем ниже влажность, тем интенсивнее идёт испарение воды из ткани, тем сильнее охлаждается резервуар ¾мокрого¿ термометра, и тем больше разность его показаний и показаний сухого термометра. По этой разности с помощью специальной психрометрической таблицы определяют влажность воздуха.
Наверняка многим приходилось наблюдать картину, как стоящая открытой емкость с водой через некоторое время оказывается пустой. Если же ее прикрыть крышкой, то вода никуда не девается. Причина всем известна - вода испаряется. Объяснение такому явлению простое: часть молекул воды имеет достаточно большую скорость движения для того, чтобы покинуть жидкость. Вот этот процесс перехода жидкости в газообразное состояние и называется испарением.
Другой процесс, а именно превращение пара в жидкость, называется конденсацией. Эти два процесса, испарение и конденсация, идут постоянно: часть воды испаряется, часть - конденсируется. Если объем над поверхностью воды неограничен, то преобладает процесс испарения. Испарившаяся вода удаляется, как, например, происходит над поверхностью открытой воды, и жидкость постепенно переходит в газообразное состояние - пар.
А вот если объем свободного пространства над жидкостью ограничен, то возникает несколько другая ситуация. Испарившаяся вода не может покинуть этот объем, и над поверхностью воды образуется насыщенный пар. Так называется пар, находящийся в состоянии равновесия, когда количество испарившейся воды и конденсировавшегося пара равны. Вода не убывает и не прибывает, наступает состояние равновесия между испарением и конденсацией.
Теперь мы знаем, что такое насыщенный пар, и его свойства, возможно, окажутся для нас достаточно любопытными. Мы с самого начала определили, что объем свободного пространства над поверхностью жидкости ограничен. Над ней образовался насыщенный пар. А если теперь этот свободный объем уменьшить? Что будет? В этом случае установившееся равновесие между конденсацией и испарением нарушится. Начнет преобладать процесс конденсации, объем влаги увеличится, а пара - уменьшится.
Давление пара, при котором он находится в равновесии с жидкостью, называется Если мы уменьшаем объем свободного пространства над водой, то давление пара увеличивается. Следствием этого и будет переход пара в воду. При увеличенном занимает меньше места, чем насыщенный пар. Из этого следует еще один вывод: если температура постоянна, то давление насыщенного пара при любом объеме одинаково.
Существует еще один вариант поведения пара - объем над поверхностью воды уменьшают, а переход пара в жидкость не происходит. Значит, над поверхностью находится ненасыщенный пар. В дальнейшем, при уменьшении объема при постоянной температуре, пар начинает превращаться в воду - значит, образовался насыщенный пар. Но не зря было оговорено условие, что все происходит при постоянной температуре. Существует определенное ее значение, при котором пар может превратиться в жидкость.
Это значение называется критической температурой. Вещество остается газом при температуре выше критической, если же она ниже критической, то газ превращается в жидкость. Каждое вещество имеет свое значение Стоит отметить еще две особенности пара: он может быть как влажный, так и сухой насыщенный пар. Во влажном присутствуют капли воды, а сухой пар не содержит влаги.
Существует еще так называемый перегретый пар - это сухой пар с температурой выше критической. В этом случае считается, что в замкнутом объеме уже нет жидкости, а присутствует исключительно пар. Перегретый пар в основном используется в технике и энергетике. перегретого пара позволяет транспортировать его с помощью паропроводов и использовать в Благодаря отсутствию воды в перегретом паре срок службы турбины увеличивается.
В статье рассмотрено, что собой представляет насыщенный пар, его виды и свойства, а также процесс его образования и превращения в жидкость.